研究人员开发了一种新的可注射纳米颗粒生成技术,可以将癌症药物输送到转移性乳腺癌细胞的细胞核。
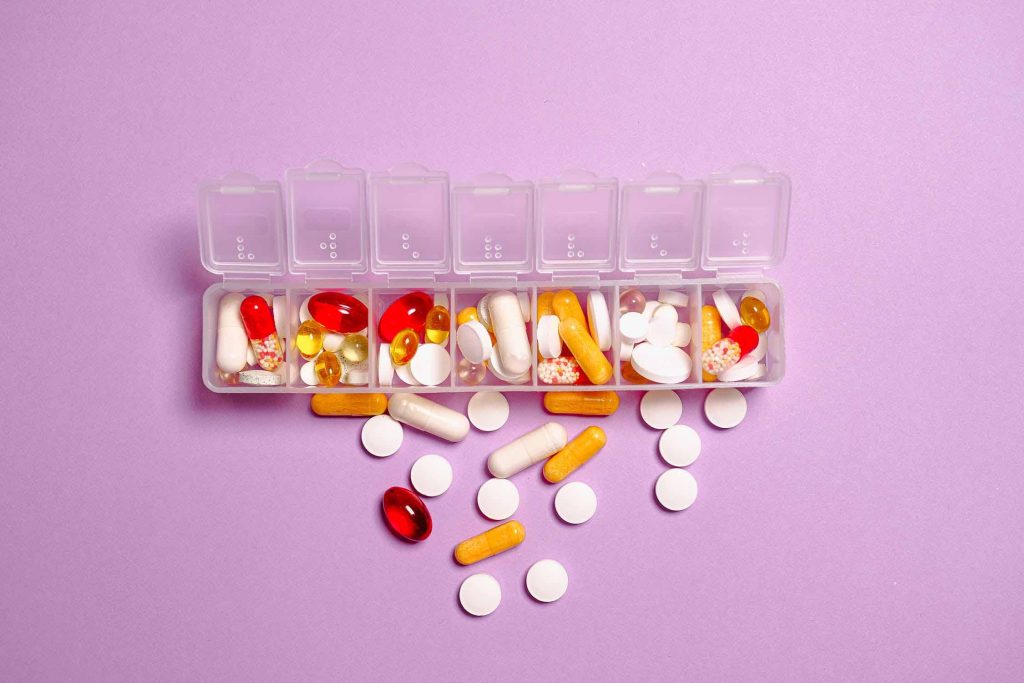
红血球(蓝色箭头)与附着在肿瘤微血管上的iNPG-pDox纳米粒子(红色箭头)相邻。
功劳:休斯顿卫理公会研究所
博士沈海发研究人员开发并测试了一种新的可注射纳米颗粒生成技术,该技术可输送阿霉素(Adriamycin?),一种常用的化疗药物,直接作用于转移性乳腺癌细胞核具有很高的疗效。
在本研究中,这种治疗方法导致小鼠完全缓解,成为一种难治疗的乳腺癌。这一发现发表在3月14日的《自然生物技术》杂志上。领导这项研究的研究团队希望在2017年底前开始在人类临床试验中测试这种疗法。
大多数化疗和靶向治疗药物的有效性受到保护癌细胞的生物屏障的限制,包括肿瘤血管壁和肿瘤细胞膜中的分子泵,休斯顿卫理公会研究所的高级研究员沈海发博士说:
“通常,不到0.1%的药物分子最终进入癌组织,而超过99.9%的药物分子留在健康组织中。”。“当肿瘤细胞接受(这样的)一种次优剂量的药物时,它们会逐渐适应并产生耐药性,”他说,
是为了增加药物的效力和减少癌细胞产生耐药性的机会,研究人员开发了一种基于纳米技术的疗法,他们称之为可注射纳米颗粒发生器(iNPG),它可以将药物通过肿瘤血管直接输送到肿瘤细胞的细胞核。
沈博士解释说,iNPG就像一个“母舰”,研究人员在其中隐藏了含有称为pDox的纳米粒的阿霉素。pDox是阿霉素分子附着在其上的长链。他指出,由于iNPG颗粒的大小和形状以及其他特性,iNPG颗粒优先聚集在乳腺癌转移的肺和肝原发部位。
一旦iNPG颗粒到达肿瘤血管,pDox纳米颗粒就会从iNPG的纳米孔中释放出来。热力学力使pDox链包裹成球状,使其类似于胞外小体,由细胞交换的膜结合囊。将纳米颗粒伪装成外显体可以让药物被肿瘤细胞吸收,并避免它们的外排泵。
一旦进入肿瘤细胞,pDox颗粒最终会流向细胞核附近的小泡,称为内质体,当内体的高pH值导致阿霉素分离并杀死细胞时,
研究人员在转移性三阴性乳腺癌小鼠模型中测试了iNPG颗粒。一半的老鼠完全缓解了病情,并且只要健康的小白鼠与小白鼠相匹配,就可以无病生存。另一半最终死于转移性疾病,但仍比用标准阿霉素或脂质体阿霉素(Doxil?)治疗的小鼠活得长得多。
“当我们做实验时,我们被震惊了,所以我们一次又一次地这样做,”休斯顿卫理公会研究所总裁兼首席执行官Mauro Ferrari博士说研究的高级研究员。“这已经是5年的动物研究了。”
费拉里博士强调说,这种方法是一种使用纳米技术的新方法。
“如果我们服用相同的[pDox]纳米颗粒,并通过静脉滴注的方式将其注射到全身循环中,它们就没有治疗效果,”他说。“关键的发现是在这些纳米颗粒到达肿瘤微环境后制造出来。”
将pDOX包装在iNPG中,使药物能够越过常常阻止肿瘤药物积聚的“生物屏障”,费拉里博士继续说道,例如那些将药物转移到非靶器官或预防肿瘤药物的屏障它离开循环进入肿瘤微环境pe、
阿霉素是目前应用最广泛的化疗药物之一。它通常用于治疗乳腺癌、卵巢癌、肉瘤和其他类型的癌症。但是阿霉素会损害心脏,所以在一个病人出现心脏副作用之前,他们可以接受的药物量是有限制的,沈博士解释说,
在研究中,在治疗后一周,接受iNPG治疗的小鼠心脏组织中没有药物的证据,也没有心脏损伤的证据,虽然接受标准阿霉素或未包装在iNPG中的pDox纳米粒的小鼠心脏中的药物水平仍然升高,并且对心脏组织造成损伤。
“有了这个平台,我们可以改变药物的生物分布,NCI纳米技术研究办公室主任Piotr Grodzinski博士说:“沈博士说,”
这种方法“无疑代表了一种独创的纳米技术。”。“很有意思的是,看看这个策略是否可以推广,以及粒子是否可以被设计成肺和肝以外的靶组织。”
费拉里博士和他的同事正在寻求食品和药物管理局的许可,以进行一期临床试验,他们希望在未来12到18年内开始几个月,他说